Ngày nay, khái niệm PRP lần đầu tiên xuất hiện trong lĩnh vực huyết học vào những năm 1970.Các nhà huyết học đã tạo ra thuật ngữ PRP cách đây nhiều thập kỷ để mô tả huyết tương thu được từ số lượng tiểu cầu cao hơn giá trị cơ bản của máu ngoại vi.Hơn mười năm sau, PRP được sử dụng trong phẫu thuật hàm mặt dưới dạng fibrin giàu tiểu cầu (PRF).Hàm lượng fibrin trong dẫn xuất PRP này có giá trị quan trọng do tính bám dính và đặc tính ở trạng thái ổn định, trong khi PRP có đặc tính chống viêm bền vững và kích thích tăng sinh tế bào.Cuối cùng, vào khoảng những năm 1990, PRP bắt đầu trở nên phổ biến.Cuối cùng, công nghệ này đã được chuyển giao sang các lĩnh vực y tế khác.Kể từ đó, loại sinh học tích cực này đã được nghiên cứu và áp dụng rộng rãi để điều trị các chấn thương cơ xương khác nhau của các vận động viên chuyên nghiệp, điều này càng thúc đẩy sự chú ý rộng rãi của nó trên các phương tiện truyền thông.Ngoài hiệu quả trong chỉnh hình và y học thể thao, PRP còn được sử dụng trong nhãn khoa, phụ khoa, tiết niệu và tim mạch, nhi khoa và phẫu thuật thẩm mỹ.Trong những năm gần đây, PRP còn được các bác sĩ da liễu đánh giá cao về tiềm năng điều trị loét da, chữa sẹo, tái tạo mô, trẻ hóa da và thậm chí là rụng tóc.
Xem xét thực tế rằng PRP có thể trực tiếp điều khiển quá trình chữa lành và viêm nhiễm, cần phải giới thiệu tầng chữa bệnh làm tài liệu tham khảo.Quá trình chữa bệnh được chia thành bốn giai đoạn sau: cầm máu;Viêm;Tăng sinh tế bào và ma trận, cuối cùng là tái tạo vết thương.
Chữa lành mô
Phản ứng xếp tầng chữa lành mô được kích hoạt, dẫn đến kết tập tiểu cầu. Sự hình thành cục máu đông và phát triển ma trận ngoại bào tạm thời (ECM).Sau đó, tiểu cầu bám vào collagen và protein ECM tiếp xúc, kích hoạt giải phóng các phân tử hoạt tính sinh học có trong hạt a.Tiểu cầu chứa nhiều phân tử hoạt tính sinh học, bao gồm các yếu tố tăng trưởng, yếu tố hóa trị và cytokine, cũng như các chất trung gian gây viêm, như prostaglandin, cyclin tuyến tiền liệt, histamine, Thromboxane, serotonin và bradykinin.
Giai đoạn cuối cùng của quá trình chữa lành phụ thuộc vào việc tái tạo vết thương.Việc tái tạo mô được quy định chặt chẽ để thiết lập sự cân bằng giữa các phản ứng đồng hóa và dị hóa.Ở giai đoạn này, yếu tố tăng trưởng có nguồn gốc từ tiểu cầu (PDGF) và yếu tố tăng trưởng biến đổi (TGF-β) Fibronectin và fibronectin kích thích sự tăng sinh và di chuyển của nguyên bào sợi, cũng như tổng hợp các thành phần ECM.Tuy nhiên, thời gian trưởng thành của vết thương phụ thuộc phần lớn vào mức độ nghiêm trọng của vết thương, đặc điểm cá nhân và khả năng chữa lành cụ thể của mô bị thương.Một số yếu tố sinh lý bệnh và chuyển hóa có thể ảnh hưởng đến quá trình chữa lành, chẳng hạn như thiếu máu cục bộ mô, thiếu oxy, nhiễm trùng, mất cân bằng yếu tố tăng trưởng và thậm chí cả các bệnh liên quan đến hội chứng chuyển hóa.
Môi trường vi mô gây viêm cản trở quá trình chữa bệnh.Phức tạp hơn là hoạt tính protease cao sẽ ức chế hoạt động tự nhiên của yếu tố tăng trưởng (GF).Ngoài các đặc tính phân bào, tạo mạch và hóa học, PRP còn là nguồn cung cấp nhiều yếu tố tăng trưởng.Những phân tử sinh học này có thể chống lại tác động có hại trong các mô viêm bằng cách kiểm soát tình trạng viêm gia tăng và thiết lập các kích thích đồng hóa.Xem xét những đặc điểm này, các nhà nghiên cứu có thể tìm thấy tiềm năng lớn trong việc điều trị các vết thương phức tạp khác nhau.
Nhiều bệnh, đặc biệt là các bệnh về cơ xương khớp, phụ thuộc rất nhiều vào các sản phẩm sinh học điều chỉnh quá trình viêm, chẳng hạn như PRP để điều trị viêm xương khớp.Trong trường hợp này, sức khỏe của sụn khớp phụ thuộc vào sự cân bằng chính xác của các phản ứng đồng hóa và dị hóa.Với nguyên tắc này, việc sử dụng một số tác nhân sinh học tích cực có thể thành công trong việc đạt được sự cân bằng lành mạnh.PRP vì nó giải phóng tiểu cầu α- Các yếu tố tăng trưởng có trong hạt được sử dụng rộng rãi để điều chỉnh khả năng biến đổi mô, từ đó cũng làm giảm đau.Trên thực tế, một trong những mục tiêu chính của điều trị PRP là ngăn chặn môi trường vi mô gây viêm và dị hóa chính, đồng thời thúc đẩy quá trình chuyển đổi sang thuốc chống viêm.Các tác giả khác trước đây đã chứng minh rằng PRP hoạt hóa bằng Thrombin làm tăng giải phóng một số phân tử sinh học.Những yếu tố này bao gồm yếu tố tăng trưởng tế bào gan (HGF) và yếu tố hoại tử khối u (TNF-α), yếu tố tăng trưởng chuyển dạng beta1 (TGF-β 1), yếu tố tăng trưởng nội mô mạch máu (VEGF) và yếu tố tăng trưởng biểu bì (EGF).Các nghiên cứu khác đã chỉ ra rằng PRP thúc đẩy sự gia tăng nồng độ collagen loại ii và mRNA aggrecan, đồng thời làm giảm sự ức chế của cytokine interleukin – (IL) 1 gây viêm trên chúng.Người ta cũng đề xuất rằng do HGF và TNF-α [28] PRP có thể giúp thiết lập tác dụng chống viêm.Cả hai chế phẩm phân tử này đều làm giảm hoạt tính và biểu hiện kháng kích hoạt của yếu tố hạt nhân kappaB (NF- κВ);Thứ hai, thông qua biểu hiện TGF-β1 còn ngăn cản sự hóa ứng động của bạch cầu đơn nhân, từ đó làm mất tác dụng của TNF-α đối với quá trình tương tác của các chemokine.HGF dường như đóng một vai trò không thể thiếu trong tác dụng chống viêm do PRP gây ra.Cytokine chống viêm mạnh này phá hủy đường truyền tín hiệu NF-κB và biểu hiện cytokine tiền viêm sẽ ức chế phản ứng viêm.Ngoài ra, PRP còn có thể làm giảm nồng độ oxit nitric (NO) cao.Ví dụ, trong sụn khớp, sự gia tăng nồng độ NO đã được chứng minh là có tác dụng ức chế tổng hợp collagen và gây ra hiện tượng chết tế bào sụn, đồng thời làm tăng tổng hợp metallicoproteinase ma trận (MMP), từ đó thúc đẩy quá trình chuyển đổi quá trình dị hóa.Về mặt thoái hóa tế bào, PRP cũng được coi là có khả năng điều khiển quá trình tự thực của các loại tế bào cụ thể.Khi đạt đến trạng thái lão hóa cuối cùng, một số nhóm tế bào mất đi khả năng ở trạng thái tĩnh và khả năng tự đổi mới.Tuy nhiên, các nghiên cứu gần đây đã chỉ ra rằng điều trị PRP có thể đảo ngược tốt các tình trạng có hại này.Moussa và các đồng nghiệp đã chứng minh rằng PRP có thể tạo ra sự bảo vệ tế bào sụn bằng cách tăng khả năng tự thực bào và các dấu hiệu chống viêm, đồng thời làm giảm quá trình tự hủy của sụn viêm xương khớp ở người.Garcia Pratt và cộng sự.Được biết, quá trình tự thực bào quyết định sự chuyển đổi giữa số phận nghỉ ngơi và lão hóa của tế bào gốc cơ.Các nhà nghiên cứu tin rằng, trong cơ thể, việc bình thường hóa quá trình tự thực bào tích hợp sẽ tránh được sự tích tụ tổn thương nội bào và ngăn ngừa sự lão hóa và suy giảm chức năng của các tế bào vệ tinh.Ngay cả trong các tế bào gốc của con người đang bị lão hóa, chẳng hạn như gần đây, Parrish và Rodes cũng đã có những đóng góp đáng kể, tiết lộ thêm về khả năng chống viêm của PRP.Lần này, trọng tâm là sự tương tác giữa tiểu cầu và bạch cầu trung tính.Trong cuộc điều tra của họ, các nhà nghiên cứu giải thích rằng các tiểu cầu được kích hoạt do axit arachidonic giải phóng đã được bạch cầu trung tính hấp thụ và chuyển đổi thành leukotrienes và prostaglandin, là những phân tử gây viêm được biết đến.Tuy nhiên, sự tương tác bạch cầu trung tính tiểu cầu cho phép chuyển đổi leukotriene thành lipoprotein, đã được chứng minh là một loại protein chống viêm hiệu quả có thể hạn chế sự kích hoạt của bạch cầu trung tính và ngăn chặn quá trình lọc máu, đồng thời thúc đẩy sự di truyền đến giai đoạn cuối của quá trình chữa lành.
Môi trường vi mô gây viêm cản trở quá trình chữa bệnh.Phức tạp hơn là hoạt tính protease cao sẽ ức chế hoạt động tự nhiên của yếu tố tăng trưởng (GF).Ngoài các đặc tính phân bào, tạo mạch và hóa học, PRP còn là nguồn cung cấp nhiều yếu tố tăng trưởng.Những phân tử sinh học này có thể chống lại tác động có hại trong các mô viêm bằng cách kiểm soát tình trạng viêm gia tăng và thiết lập sự kích thích đồng hóa.
Yếu tố tế bào
Cytokine trong PRP đóng vai trò chính trong việc điều khiển quá trình sửa chữa mô và điều chỉnh tổn thương do viêm.Các cytokine chống viêm là một loạt các phân tử sinh hóa làm trung gian cho phản ứng của các cytokine tiền viêm, chủ yếu được gây ra bởi các đại thực bào được kích hoạt.Các cytokine chống viêm tương tác với các chất ức chế cytokine cụ thể và các thụ thể cytokine hòa tan để điều chỉnh tình trạng viêm.Interleukin (IL) – 1 chất đối kháng thụ thể IL-4, IL-10, IL-11 và IL-13 được phân loại là thuốc chống viêm chính, cytokine.Tùy theo các loại vết thương khác nhau, một số cytokine, chẳng hạn như interferon, yếu tố ức chế bệnh bạch cầu, TGF-β và IL-6, có thể cho thấy tác dụng tiền viêm hoặc chống viêm.TNF-α, IL-1 và IL-18 có một số thụ thể cytokine nhất định, có thể ức chế tác dụng gây viêm của các protein khác [37].IL-10 là một trong những cytokine chống viêm hiệu quả nhất, có thể điều chỉnh giảm các cytokine tiền viêm như IL-1, IL-6 và TNF-α, đồng thời điều chỉnh các yếu tố chống viêm.Các cơ chế chống điều hòa này đóng một vai trò quan trọng trong việc sản xuất và chức năng của các cytokine tiền viêm.Ngoài ra, một số cytokine nhất định có thể kích hoạt các phản ứng tín hiệu cụ thể để kích thích các nguyên bào sợi, điều này rất quan trọng cho việc sửa chữa mô.Cytokine gây viêm TGF β 1, IL-1 β, IL-6, IL-13 và IL-33 kích thích các nguyên bào sợi biệt hóa thành nguyên bào sợi cơ và cải thiện ECM [38].Đổi lại, các nguyên bào sợi tiết ra các chemokine cytokine TGF- β, IL-1 β, IL-33, CXC và CC thúc đẩy phản ứng viêm bằng cách kích hoạt và tuyển dụng các tế bào miễn dịch như đại thực bào.Các tế bào viêm này đóng nhiều vai trò trong vết thương, chủ yếu bằng cách thúc đẩy quá trình làm sạch vết thương - và sinh tổng hợp chemokine, chất chuyển hóa và các yếu tố tăng trưởng, rất quan trọng cho việc tái tạo các mô mới.Vì vậy, các cytokine trong PRP đóng vai trò quan trọng trong việc kích thích đáp ứng miễn dịch qua trung gian loại tế bào và thúc đẩy quá trình thoái lui của giai đoạn viêm.Trên thực tế, một số nhà nghiên cứu đã gọi quá trình này là "viêm tái tạo", chỉ ra rằng giai đoạn viêm, bất chấp sự lo lắng của bệnh nhân, là một bước cần thiết và quan trọng để kết thúc thành công quá trình sửa chữa mô, có tính đến cơ chế biểu sinh mà tín hiệu viêm thúc đẩy tính dẻo của tế bào.
Vai trò của cytokine trong tình trạng viêm da của thai nhi có ý nghĩa rất lớn đối với việc nghiên cứu y học tái tạo.Sự khác biệt giữa cơ chế chữa lành của thai nhi và người trưởng thành là các mô của thai nhi bị tổn thương đôi khi trở lại trạng thái ban đầu tùy theo tuổi của thai nhi và các loại mô liên quan.Ở người, da của thai nhi có thể tái tạo hoàn toàn trong vòng 24 tuần, trong khi ở người lớn, vết thương mau lành có thể dẫn đến hình thành sẹo.Như chúng ta đã biết, so với các mô khỏe mạnh, tính chất cơ học của mô sẹo giảm đáng kể và chức năng của chúng bị hạn chế.Đặc biệt chú ý đến cytokine IL-10, được phát hiện có nhiều trong nước ối và da thai nhi, và đã được chứng minh là có vai trò trong việc phục hồi da thai nhi không bị sẹo, được thúc đẩy nhờ tác dụng đa hướng của cytokine.ZgheibC và cộng sự.Việc cấy ghép da của thai nhi vào chuột IL-10 biến đổi gen (KO) và chuột đối chứng đã được nghiên cứu.Chuột IL-10KO có dấu hiệu viêm và hình thành sẹo xung quanh mảnh ghép, trong khi mảnh ghép ở nhóm đối chứng cho thấy không có thay đổi đáng kể về đặc tính cơ sinh học và không lành sẹo.
Tầm quan trọng của việc điều chỉnh sự cân bằng mong manh giữa sự biểu hiện của các cytokine chống viêm và gây viêm là khi các cytokine gây viêm được sản xuất quá mức, cuối cùng sẽ gửi tín hiệu về sự thoái hóa tế bào bằng cách giảm sự biểu hiện của một số gen nhất định.Ví dụ, trong y học cơ xương khớp, IL-1 β Down điều hòa SOX9, chất chịu trách nhiệm phát triển sụn.SOX9 tạo ra các yếu tố phiên mã quan trọng cho sự phát triển của sụn, điều hòa collagen loại II alpha 1 (Col2A1) và chịu trách nhiệm mã hóa các gen collagen loại II.IL-1 β Cuối cùng, sự biểu hiện của Col2A1 và aggrecan đã giảm đi.Tuy nhiên, điều trị bằng các sản phẩm giàu tiểu cầu đã được chứng minh là có tác dụng ức chế IL-1 β. Đây vẫn là một đồng minh khả thi của y học tái tạo để duy trì sự biểu hiện của các gen mã hóa collagen và làm giảm quá trình tự hủy của tế bào sụn do các cytokine tiền viêm gây ra.
Kích thích đồng hóa: Ngoài việc điều chỉnh trạng thái viêm của mô bị tổn thương, các cytokine trong PRP còn tham gia vào phản ứng đồng hóa bằng cách đóng vai trò nguyên phân, thu hút hóa học và tăng sinh.Đây là một nghiên cứu in vitro do Cavallo et al.Để nghiên cứu tác dụng của các PRP khác nhau đối với tế bào sụn của con người.Các nhà nghiên cứu quan sát thấy rằng các sản phẩm PRP có nồng độ tiểu cầu và bạch cầu tương đối thấp sẽ kích thích hoạt động bình thường của tế bào sụn, điều này có lợi cho việc thúc đẩy một số cơ chế tế bào của phản ứng đồng hóa.Ví dụ, người ta đã quan sát thấy sự biểu hiện của collagen loại ii và glycans tổng hợp.Ngược lại, nồng độ cao của tiểu cầu và bạch cầu dường như kích thích các con đường truyền tín hiệu tế bào khác liên quan đến nhiều loại cytokine khác nhau.Các tác giả cho rằng điều này có thể là do sự hiện diện của một số lượng lớn tế bào bạch cầu trong công thức PRP đặc biệt này.Những tế bào này dường như chịu trách nhiệm làm tăng biểu hiện của một số yếu tố tăng trưởng nhất định, chẳng hạn như VEGF, FGF-b và interleukin IL-1b và IL-6, từ đó có thể kích thích TIMP-1 và IL-10.Nói cách khác, so với công thức PRP “xấu”, hỗn hợp PRP giàu tiểu cầu và bạch cầu dường như phát huy khả năng xâm lấn tương đối của tế bào sụn.
Một nghiên cứu được thiết kế bởi Schnabel et al.được thiết kế để đánh giá vai trò của vật liệu sinh học tự thân trong mô gân ngựa.Các tác giả đã thu thập mẫu máu và gân từ sáu con ngựa trưởng thành (2-4 tuổi) và tập trung nghiên cứu mô hình biểu hiện gen, hàm lượng DNA và collagen của mẫu mô gân của flexor Digitorum surfaceis của ngựa được nuôi cấy trong môi trường chứa PRP. hoặc các sản phẩm máu khác.Mẫu mô gân được nuôi cấy trong máu, huyết tương, PRP, huyết tương thiếu tiểu cầu (PPP) hoặc dịch hút tủy xương (BMA), và các axit amin được thêm vào 100%, 50% hoặc 10% DMEM không có huyết thanh.Khi tiến hành phân tích sinh hóa có thể áp dụng sau…, các nhà nghiên cứu lưu ý rằng TGF- β Nồng độ PDGF-BB và PDGF-1 trong môi trường PRP đặc biệt cao hơn so với tất cả các sản phẩm máu khác được thử nghiệm.Ngoài ra, các mô gân được nuôi cấy trong môi trường 100% PRP cho thấy sự biểu hiện gen của protein ma trận COL1A1, COL3A1 và COMP tăng lên, nhưng không làm tăng các enzyme dị hóa MMPs3 và 13. Ít nhất về mặt cấu trúc gân, nghiên cứu in vivo này hỗ trợ việc sử dụng autolo – một sản phẩm máu bệnh gút, hay PRP, để điều trị viêm gân động vật có vú lớn.
Chen và cộng sự.Hiệu quả tái tạo của PRP đã được thảo luận thêm.Trong loạt nghiên cứu trước đây, các nhà nghiên cứu đã chứng minh rằng, ngoài việc tăng cường hình thành sụn, PRP còn thúc đẩy tăng tổng hợp ECM và ức chế phản ứng viêm của sụn khớp và nhân nhầy.PRP có thể kích hoạt TGF thông qua quá trình phosphoryl hóa Smad2/3- β Con đường tín hiệu đóng vai trò quan trọng trong sự phát triển và biệt hóa tế bào.Ngoài ra, người ta cũng tin rằng các cục fibrin hình thành sau khi kích hoạt PRP cung cấp cấu trúc ba chiều vững chắc, cho phép các tế bào bám dính, điều này có thể dẫn đến việc hình thành các mô mới.
Các nhà nghiên cứu khác đã có những đóng góp đáng kể trong việc điều trị loét da mãn tính trong lĩnh vực da liễu.Điều này cũng đáng chú ý.Ví dụ, nghiên cứu do Hessler và Shyam thực hiện vào năm 2019 cho thấy PRP có giá trị như một phương pháp điều trị thay thế khả thi và hiệu quả, trong khi bệnh loét mãn tính kháng thuốc vẫn mang lại gánh nặng kinh tế đáng kể cho việc chăm sóc sức khỏe.Đặc biệt, loét bàn chân do tiểu đường là một vấn đề sức khỏe lớn được nhiều người biết đến, khiến chân tay dễ bị cắt cụt.Một nghiên cứu được công bố bởi Ahmed et al.năm 2017 cho thấy gel PRP tự thân có thể kích thích quá trình lành vết thương ở bệnh nhân loét bàn chân do tiểu đường mãn tính bằng cách giải phóng các yếu tố tăng trưởng cần thiết, từ đó cải thiện đáng kể tỷ lệ lành vết thương.Tương tự, Gonchar và các đồng nghiệp đã xem xét và thảo luận về tiềm năng tái tạo của PRP và các loại cocktail chứa yếu tố tăng trưởng trong việc cải thiện việc điều trị loét bàn chân do tiểu đường.Các nhà nghiên cứu đề xuất rằng việc sử dụng hỗn hợp yếu tố tăng trưởng có thể là một giải pháp khả thi, có thể cải thiện những ưu điểm của việc sử dụng PRP và yếu tố tăng trưởng đơn lẻ.Do đó, so với việc sử dụng yếu tố tăng trưởng đơn lẻ, sự kết hợp giữa PRP và các chiến lược điều trị khác có thể thúc đẩy đáng kể quá trình lành vết loét mãn tính.
fibrin
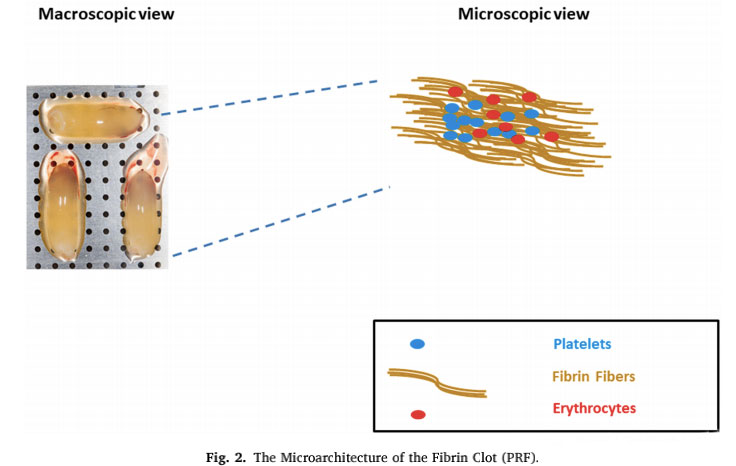
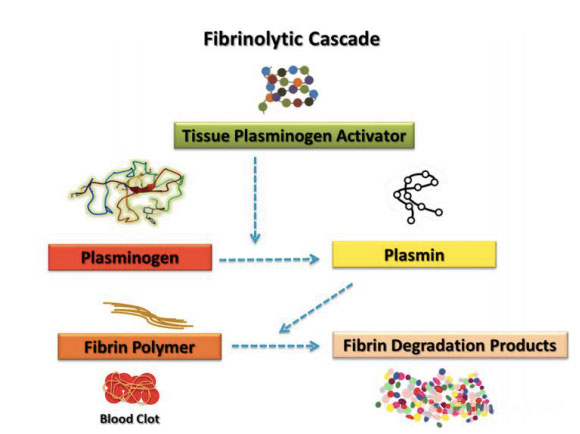
Tiểu cầu mang một số yếu tố liên quan đến hệ thống tiêu sợi huyết, có thể điều chỉnh tăng hoặc giảm điều hòa phản ứng tiêu sợi huyết.Mối quan hệ về thời gian và sự đóng góp tương đối của các thành phần huyết học và chức năng tiểu cầu trong quá trình thoái hóa cục máu đông vẫn là vấn đề đáng được thảo luận rộng rãi trong cộng đồng.Tài liệu giới thiệu nhiều nghiên cứu chỉ tập trung vào tiểu cầu, vốn nổi tiếng với khả năng ảnh hưởng đến quá trình chữa bệnh.Mặc dù có rất nhiều nghiên cứu nổi bật, các thành phần huyết học khác, chẳng hạn như các yếu tố đông máu và hệ thống tiêu sợi huyết, cũng đã được chứng minh là góp phần đáng kể vào việc sửa chữa vết thương hiệu quả.Theo định nghĩa, tiêu sợi huyết là một quá trình sinh học phức tạp phụ thuộc vào sự kích hoạt của một số enzyme để thúc đẩy sự thoái hóa của fibrin.Phản ứng tiêu sợi huyết đã được các tác giả khác đề xuất rằng các sản phẩm thoái hóa fibrin (fdp) thực sự có thể là tác nhân phân tử chịu trách nhiệm kích thích sửa chữa mô.Chuỗi các sự kiện sinh học quan trọng trước đây là từ sự lắng đọng fibrin và loại bỏ sự hình thành mạch, cần thiết cho quá trình lành vết thương.Sự hình thành cục máu đông sau chấn thương đóng vai trò như một lớp bảo vệ để bảo vệ các mô khỏi mất máu và sự xâm nhập của các tác nhân vi sinh vật, đồng thời cung cấp một ma trận tạm thời để các tế bào có thể di chuyển trong quá trình sửa chữa.Cục máu đông là do fibrinogen bị phân cắt bởi serine protease và tiểu cầu được tập hợp trong lưới sợi fibrin liên kết ngang.Phản ứng này kích hoạt sự trùng hợp của monome fibrin, đây là sự kiện chính hình thành cục máu đông.Cục máu đông cũng có thể được sử dụng như một nơi chứa các cytokine và các yếu tố tăng trưởng, được giải phóng trong quá trình thoái hóa tiểu cầu đã hoạt hóa.Hệ thống tiêu sợi huyết được điều hòa chặt chẽ bởi plasmin và đóng vai trò chính trong việc thúc đẩy di chuyển tế bào, khả dụng sinh học của các yếu tố tăng trưởng và điều hòa các hệ thống protease khác liên quan đến viêm và tái tạo mô.Các thành phần chính của quá trình tiêu sợi huyết, chẳng hạn như thụ thể hoạt hóa plasminogen urokinase (uPAR) và chất ức chế hoạt hóa plasminogen-1 (PAI-1), được biết là biểu hiện trong tế bào gốc trung mô (MSC), là loại tế bào đặc biệt cần thiết để chữa lành vết thương thành công. .
Di chuyển tế bào
Kích hoạt plasminogen thông qua liên kết uPA uPAR là một quá trình thúc đẩy sự di chuyển của các tế bào viêm vì nó giúp tăng cường quá trình phân giải protein ngoại bào.Do thiếu các miền xuyên màng và nội bào, uPAR cần các thụ thể đồng như integrin và vitellin để điều chỉnh sự di chuyển của tế bào.Nó còn chỉ ra rằng sự gắn kết của uPA uPAR dẫn đến sự gia tăng ái lực của uPAR với vitrectectin và integrin, giúp thúc đẩy sự kết dính của tế bào.Chất ức chế hoạt hóa Plasminogen-1 (PAI-1) lần lượt làm cho các tế bào tách ra.Khi liên kết với uPA của phức hợp uPA upar integrin trên bề mặt tế bào, nó sẽ phá hủy sự tương tác giữa upar vitellin và integrin vitellin.
Trong bối cảnh y học tái tạo, tế bào gốc trung mô tủy xương được huy động từ tủy xương trong trường hợp tổn thương cơ quan nghiêm trọng, vì vậy chúng có thể được tìm thấy trong tuần hoàn của bệnh nhân bị gãy xương nhiều lần.Tuy nhiên, trong những trường hợp cụ thể, chẳng hạn như suy thận giai đoạn cuối, suy gan giai đoạn cuối hoặc trong quá trình đào thải sau ghép tim, những tế bào này có thể không được phát hiện trong máu [66].Điều thú vị là, các tế bào tiền thân trung mô (mô đệm) có nguồn gốc từ tủy xương người này không thể được phát hiện trong máu của những người khỏe mạnh [67].Vai trò của uPAR trong việc huy động tế bào gốc trung mô tủy xương (BMSC) đã được đề xuất trước đây, tương tự như sự xuất hiện của uPAR trong việc huy động tế bào gốc tạo máu (HSC).Varabaneni và cộng sự.Kết quả cho thấy việc sử dụng yếu tố kích thích tạo cụm bạch cầu hạt ở chuột thiếu uPAR đã gây ra sự thất bại của MSC, điều này một lần nữa củng cố vai trò hỗ trợ của hệ thống tiêu sợi huyết trong quá trình di chuyển tế bào.Các nghiên cứu sâu hơn cũng chỉ ra rằng các thụ thể uPA gắn với glycosyl phosphatidylinositol điều chỉnh sự bám dính, di chuyển, tăng sinh và biệt hóa bằng cách kích hoạt các con đường truyền tín hiệu nội bào nhất định, như sau: các con đường truyền tín hiệu phosphatidylinositol 4,5-diphosphate 3-kinase/Akt và ERK1/2 có thể sống sót và kinase bám dính (FAK).
Trong bối cảnh chữa lành vết thương của MSC, yếu tố tiêu sợi huyết đã chứng tỏ tầm quan trọng hơn nữa của nó.Ví dụ, những con chuột thiếu plasminogen cho thấy quá trình lành vết thương bị chậm trễ nghiêm trọng, cho thấy rằng plasmin rất quan trọng trong quá trình này.Ở người, mất plasmin cũng có thể dẫn đến các biến chứng trong quá trình lành vết thương.Sự gián đoạn lưu lượng máu có thể ức chế đáng kể quá trình tái tạo mô, điều này cũng giải thích tại sao các quá trình tái tạo này khó khăn hơn ở bệnh nhân tiểu đường.
Tế bào gốc trung mô tủy xương được tuyển dụng vào vị trí vết thương để đẩy nhanh quá trình lành vết thương.Trong điều kiện ổn định, các ô này biểu thị uPAuPAR và PAI-1.Hai protein cuối cùng là các yếu tố cảm ứng thiếu oxy α (HIF-1 α) Việc nhắm mục tiêu rất thuận tiện vì HIF-1 trong MSC α Việc kích hoạt FGF-2 và HGF đã thúc đẩy sự điều chỉnh tăng của FGF-2 và HGF;HIF-2 α Ngược lại, VEGF-A [77] được điều chỉnh tăng, cùng góp phần chữa lành vết thương.Ngoài ra, HGF dường như tăng cường việc tuyển dụng các tế bào gốc trung mô tủy xương vào các vị trí vết thương theo cách hiệp đồng.Cần lưu ý rằng tình trạng thiếu máu cục bộ và thiếu oxy đã được chứng minh là cản trở đáng kể quá trình lành vết thương.Mặc dù BMSC có xu hướng sống trong các mô cung cấp lượng oxy thấp, khả năng sống sót của BMSC được cấy ghép in vivo trở nên hạn chế do các tế bào được cấy ghép thường chết trong các điều kiện bất lợi quan sát thấy ở các mô bị tổn thương.Số phận bám dính và sống sót của tế bào gốc trung mô tủy xương trong tình trạng thiếu oxy phụ thuộc vào các yếu tố tiêu sợi huyết do các tế bào này tiết ra.PAI-1 có ái lực cao với vitellin nên có thể cạnh tranh sự gắn kết của uPAR và integrin với vitellin, do đó ức chế sự kết dính và di chuyển của tế bào.
Hệ thống bạch cầu đơn nhân và tái sinh
Theo tài liệu, có nhiều cuộc thảo luận về vai trò của bạch cầu đơn nhân trong việc chữa lành vết thương.Đại thực bào chủ yếu đến từ bạch cầu đơn nhân trong máu và đóng vai trò quan trọng trong y học tái tạo [81].Vì bạch cầu trung tính tiết ra IL-4, IL-1, IL-6 và TNF-α nên các tế bào này thường xâm nhập vào vết thương khoảng 24-48 giờ sau khi bị thương.Tiểu cầu giải phóng trombin và yếu tố tiểu cầu 4 (PF4), có thể thúc đẩy việc tuyển dụng bạch cầu đơn nhân và biệt hóa thành đại thực bào và tế bào đuôi gai.Một đặc điểm quan trọng của đại thực bào là tính dẻo của chúng, nghĩa là chúng có thể chuyển đổi kiểu hình và biệt hóa thành các loại tế bào khác, chẳng hạn như tế bào nội mô, sau đó thể hiện các chức năng khác nhau đối với các kích thích sinh hóa khác nhau trong môi trường vi mô vết thương.Các tế bào viêm biểu hiện hai kiểu hình chính, M1 hoặc M2, tùy thuộc vào tín hiệu phân tử cục bộ là nguồn kích thích.Đại thực bào M1 được tạo ra bởi các tác nhân vi sinh vật nên chúng có nhiều tác dụng gây viêm hơn.Ngược lại, đại thực bào M2 thường được tạo ra bởi các phản ứng loại 2 và có đặc tính chống viêm, đặc trưng bởi sự gia tăng IL-4, IL-5, IL-9 và IL-13.Nó cũng tham gia vào việc sửa chữa mô thông qua việc sản xuất các yếu tố tăng trưởng.Quá trình chuyển đổi từ phân nhóm M1 sang M2 phần lớn được thúc đẩy bởi giai đoạn muộn của quá trình lành vết thương.Đại thực bào M1 kích hoạt quá trình apoptosis của bạch cầu trung tính và bắt đầu quá trình thanh lọc các tế bào này).Quá trình thực bào của bạch cầu trung tính kích hoạt một loạt các sự kiện, trong đó việc sản xuất cytokine bị ngừng lại, phân cực các đại thực bào và giải phóng TGF- β 1. Yếu tố tăng trưởng này là yếu tố điều chỉnh chính cho sự biệt hóa nguyên bào sợi cơ và sự co rút của vết thương, cho phép giải quyết tình trạng viêm và sự bắt đầu của giai đoạn tăng sinh trong dòng thác chữa lành [57].Một loại protein có liên quan cao khác tham gia vào quá trình tế bào là serine (SG).Proteoglycan hạt bài tiết tế bào tạo máu này đã được phát hiện là cần thiết để lưu trữ protein bài tiết trong các tế bào miễn dịch cụ thể, chẳng hạn như tế bào mast, bạch cầu trung tính và tế bào lympho T gây độc tế bào.Mặc dù nhiều tế bào không tạo máu cũng tổng hợp plasminogen, nhưng tất cả các tế bào viêm đều sản xuất một lượng lớn protein này và lưu trữ nó ở dạng hạt để tiếp tục tương tác với các chất trung gian gây viêm khác, bao gồm protease, cytokine, chemokine và các yếu tố tăng trưởng.Chuỗi glycosaminoglycan (GAG) tích điện âm trong SG dường như rất quan trọng đối với sự ổn định của các hạt bài tiết, vì chúng có thể liên kết và tạo điều kiện thuận lợi cho việc lưu trữ các thành phần hạt tích điện cơ bản trong tế bào, protein và chuỗi GAG theo cách cụ thể.Về việc tham gia nghiên cứu PRP, Woulfe và các đồng nghiệp trước đây đã chỉ ra rằng tình trạng thiếu SG có liên quan chặt chẽ đến những thay đổi hình thái tiểu cầu;Yếu tố tiểu cầu 4 β- Khiếm khuyết dự trữ PDGF trong huyết khối và tiểu cầu;Kết tập và bài tiết tiểu cầu kém trong ống nghiệm và khiếm khuyết huyết khối trong cơ thể.Do đó, các nhà nghiên cứu kết luận rằng proteoglycan này dường như là chất điều hòa chính của huyết khối.
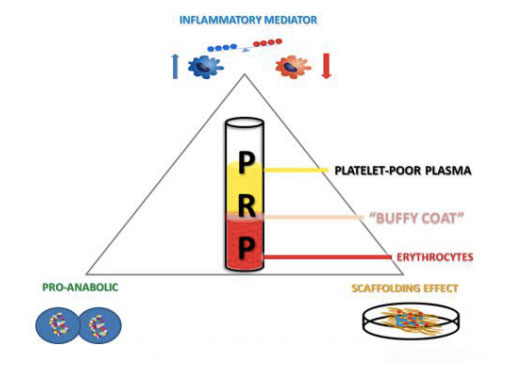
Các sản phẩm giàu tiểu cầu có thể thu được máu toàn phần của cá nhân thông qua việc thu thập và ly tâm, đồng thời chia hỗn hợp thành các lớp khác nhau chứa huyết tương, tiểu cầu, bạch cầu và bạch cầu.Khi nồng độ tiểu cầu cao hơn giá trị cơ bản, nó có thể đẩy nhanh sự phát triển của xương và mô mềm, với ít tác dụng phụ nhất.Việc ứng dụng các sản phẩm PRP tự thân là một công nghệ sinh học tương đối mới, liên tục cho thấy những kết quả lạc quan trong việc kích thích và tăng cường chữa lành các tổn thương mô khác nhau.Hiệu quả của phương pháp điều trị thay thế này có thể là do việc cung cấp tại chỗ nhiều loại yếu tố tăng trưởng và protein để mô phỏng và hỗ trợ quá trình chữa lành vết thương sinh lý và sửa chữa mô.Ngoài ra, hệ thống tiêu sợi huyết rõ ràng có ảnh hưởng quan trọng đến việc sửa chữa toàn bộ mô.Ngoài việc thay đổi việc tuyển dụng tế bào của các tế bào viêm và tế bào gốc trung mô tủy xương, nó còn có thể điều chỉnh hoạt động phân giải protein của các vùng chữa lành vết thương và quá trình tái tạo của các mô trung mô, bao gồm xương, sụn và cơ, vì vậy nó là thành phần chính của thuốc cơ xương khớp.
Tăng tốc chữa bệnh là mục tiêu được nhiều chuyên gia trong lĩnh vực y tế theo đuổi.PRP đại diện cho một công cụ sinh học tích cực, tiếp tục mang lại sự phát triển đầy hứa hẹn trong việc kích thích và điều phối chuỗi các sự kiện tái tạo.Tuy nhiên, vì công cụ trị liệu này vẫn còn rất phức tạp, đặc biệt là vì nó giải phóng vô số yếu tố hoạt tính sinh học cũng như các cơ chế tương tác và tác dụng truyền tín hiệu khác nhau của chúng nên cần phải nghiên cứu thêm.
(Nội dung của bài viết này được in lại và chúng tôi không đưa ra bất kỳ đảm bảo rõ ràng hay ngụ ý nào về tính chính xác, độ tin cậy hoặc tính đầy đủ của nội dung trong bài viết này và không chịu trách nhiệm về ý kiến của bài viết này, vui lòng hiểu.)
Thời gian đăng: 16-12-2022